
국내 신약 개발 바이오텍 6곳의 파이프라인(신약 후보물질)에 대한 우수과제 사례를 공유하는 장이 마련됐다.
10일 국가신약개발사업단(단장 박영민, KDDF)은 서울 마포구 호텔 나루 서울 엠갤러리에서 '2024 국가신약개발사업 우수과제 발표회'를 개최했다. 이번 행사는 국가신약개발사업 우수과제로 선정된 기업 6곳 관계자의 발표 및 시상식으로 구성됐다.
박영민 국가신약개발사업단장은 이날 개회사에서 "현재 신약개발사업단은 (바이오텍 지원을 위해) 열심히 준비하고 있다"며 "내년에는 임상 단계 과제에 대한 예산 규모를 30% 증액해 지원을 강화할 예정"이라고 말했다.

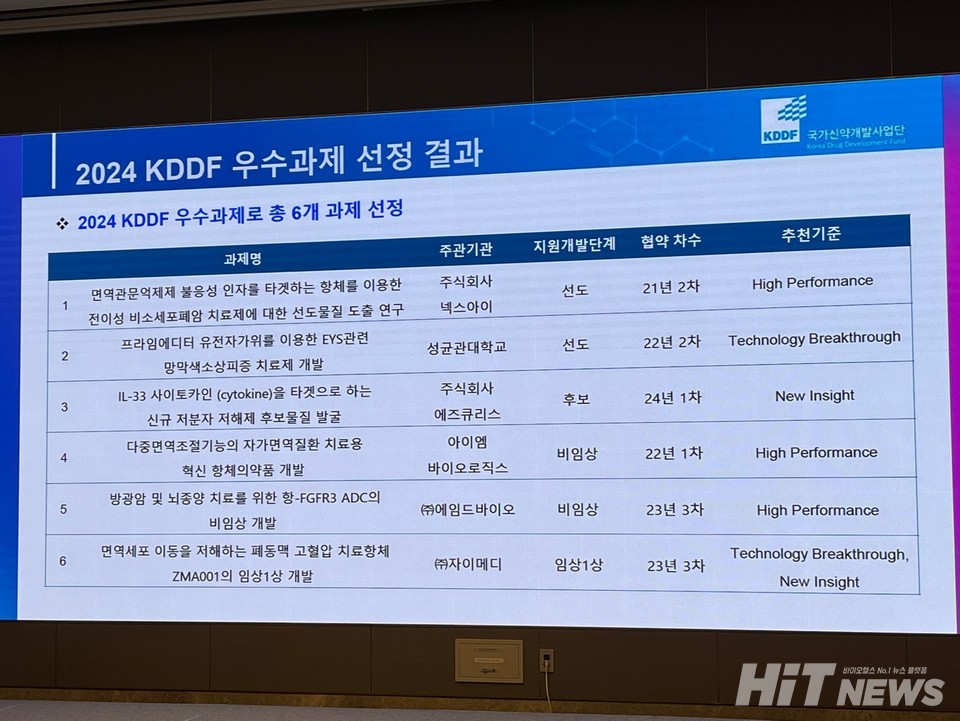
이어 마이크를 잡은 김순남 국가신약개발사업단 연구개발(R&D) 본부장은 올해 우수과제 선정에 대한 경과 보고를 발표했다. 김 본부장은 "작년에 이어 올해도 우수과제 발표회를 열었다. 앞으로 우수과제 행사를 정례화할 예정"이라며 "협약을 맺은 391개 과제 중 6개의 우수과제를 선정했다"고 밝혔다.
우수과제 선정 기준으로는 당해년도 높은 퍼포먼스(High performance), 기술 혁신(Technology breakthrough), 새로운 인사이트(New insight)에 대한 모두 혹은 어느 한쪽(and/or)의 조건 충족에 달려있다는 게 김 본부장의 설명이다.
그는 "사업단은 공정하고 객관적인 심의 절차를 통한 우수과제 선정을 진행하고 있다. 1차 내부심의 이후 외부 전문심의위원을 위촉한 뒤 2차 최종 심의를 거친다"며 "이를 바탕으로 올해 총 6개의 우수과제를 선정했다"고 전했다.
이번에 선정된 우수과제(6건) △넥스아이(면역관문억제제 불응성 인자를 타깃하는 항체를 이용한 전이성 비소세포폐암 치료제에 대한 선도물질 도출 연구) △성균관대학교 산학협력단(프라임에디터 유전자가위를 이용한 EYS 관련 망막색소상피증 치료제 개발 △에즈큐리스(IL-33 사이토카인(Cytokine)을 타깃으로 하는 신규 저분자 저해제 후보물질 발굴) △아이엠바이오로직스(다중면역조절기능의 자가면역질환 치료용 혁신 항체의약품 개발) △에임드바이오(방광암 및 뇌종양 치료를 위한 항-FGFR3 항체약물접합체(ADC)의 비임상 개발 △자이메디(면역세포 이동을 저해하는 폐동맥 고혈압 치료항체 ZMA001의 임상 1상 개발) 등이다.
아이엠바이오, 'IMB-101' 1b상 준비 중…올해 2건 L/O 체결
윤경완 넥스아이 대표 "사업단 과제 'NXI-101', 日 오노에 L/O"

하경식 아이엠바이오로직스 대표는 우수과제 발표를 통해 이중항체 기반의 자가면역질환 치료 후보물질인 'IMB-101'을 소개했다. 하 대표는 "회사는 그동안 누적 370억원 규모의 투자금을 유치했다. 올해 2건의 글로벌 기술수출(L/O) 계약을 체결했다"며 "동아ST와 ePENDY(enhanced/engineered Pentamer body) 플랫폼 기반의 항체신약 공동연구를 진행하고 있다"고 운을 뗐다.
그러면서 "지난해 3월 국가신약개발사업단으로부터 비임상 과제에 선정된 IBM-101은 염증성 싸이토카인 및 후천성 적응면역을 동시에 억제한다"며 "작년 10월 기관생명윤리위원회(IRB)서 승인을 받았고, 같은 해 12월 임상시험 투약에 나섰다"며 "최근 임상 1a상 시료 분석을 완료했고, 임상 1b상을 준비 중"이라고 덧붙였다.
하 대표의 발표에 따르면 IBM-101 약물을 투여한 피험자 30명 중에서 1건 이상의 부작용(AE)이 발생한 피험자수는 5명이지만, 약한 부작용을 나타냈다"며 "AE로 인한 임상 중단 피험자수는 없었기 때문에 임상 1a상은 성공적으로 끝났다"고 강조했다.

윤경완 넥스아이 대표는 면역항암제 후보물질 'NXI-101'의 특징 및 기술수출 사례를 설명했다. 윤 대표는 "NXI-101은 선도물질 도출을 위한 과제였다. 저희가 임상시험계획(IND)을 제출하기 전 (지난 3월) 일본 오노약품공업에 NXI-101에 대한 기술수출에 성공했다"고 말했다.
그는 "국가신약개발사업단으로부터 두 과제를 지원받았다. 그 중 첫 번째 파이프라인이 NXI-101"이라며 "NXI-101의 기술수출 대상 제약사인 오노약품공업은 브리스톨마이어스스퀴브(BMS) 옵디보(Opdivo)의 원개발사로, 연간 약 5000~7000억원의 로열티를 수령하고 있다"고 밝혔다.
오노약품공업은 작년 12여개 회사와 공동 연구 및 개발 계약을 체결했으며, 단 1건의 라이선스 인(L/I, 기술도입) 계약을 체결했다는 게 윤 대표의 설명이다. 한편 성균관대 산학협력단, 에즈큐리스, 에임드바이오, 자이메디 관계자들은 우수과제로 선정된 파이프라인의 비임상 및 임상 진행 과정 등을 소개했다.